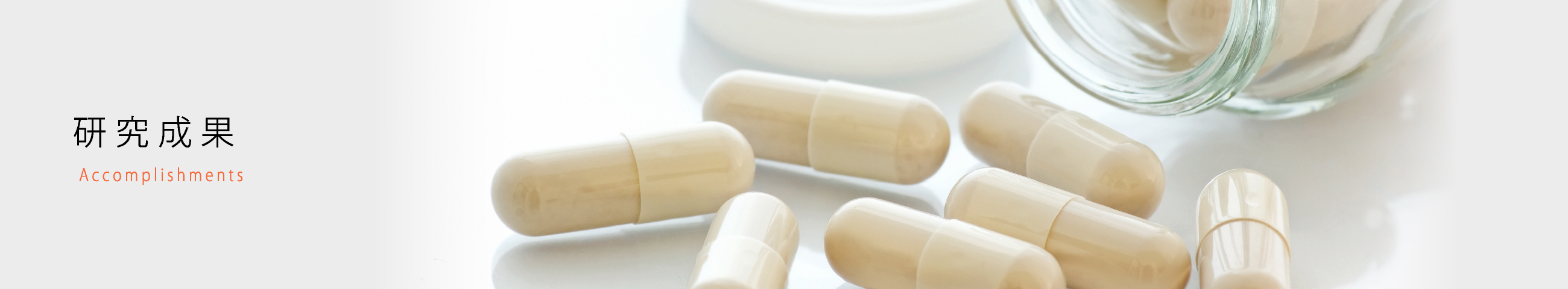
小児がんの一種であるリンパ腫
0~14歳の子どもの死亡原因のうち、がんが占める割合は全体で約1割です。しかし、5~9歳では死因の約3割を占めています。
小児がんは早期発見が難しく進行も速いのですが、成人のがんに比べて治療の効果が高いという特徴があります。
毎年、約2,100人の子どもが小児がんと診断され、そのうち約150人がリンパ腫です。リンパ腫は血液のがんの一種であり、成人のリンパ腫は毎年約36,000人がかかっています。
本研究では小児のリンパ腫の中の「ホジキンリンパ腫」と「未分化大細胞リンパ腫」を対象にしています。
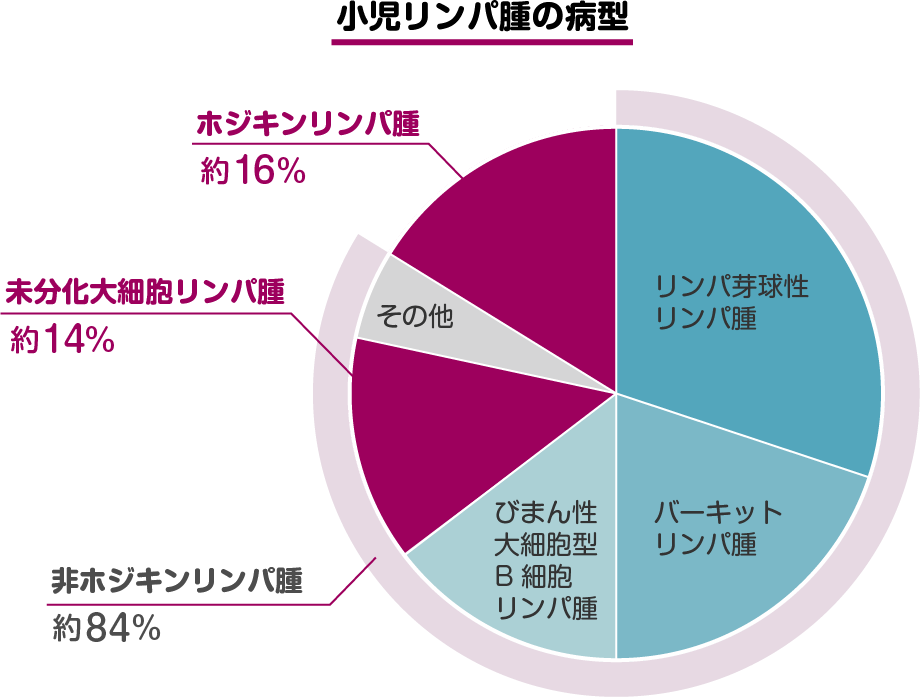
病気をどう治療するのか
「CD」というのは、血液細胞の表面に現れるタンパク質を目印として番号で分けた名前で、現在までに1~400近くもの識別番号が知られています。その中の「CD30」という番号のタンパク質は、ホジキンリンパ腫、未分化大細胞リンパ腫のがん細胞に高い頻度で現れるのが特徴です。
ブレンツキシマブ ベドチン(商品名:アドセトリス)はCD30を標的にした薬です。この薬はCD30に反応する抗体に抗がん薬を組み合わせた「抗体薬物複合体」と呼ばれるものです。CD30を目印にしてがん細胞と結合し、がん細胞の中から増殖を阻止する薬剤を放出することでがん細胞を攻撃するのです。
成人ではこの薬が標準的な治療の1つとして使われています。
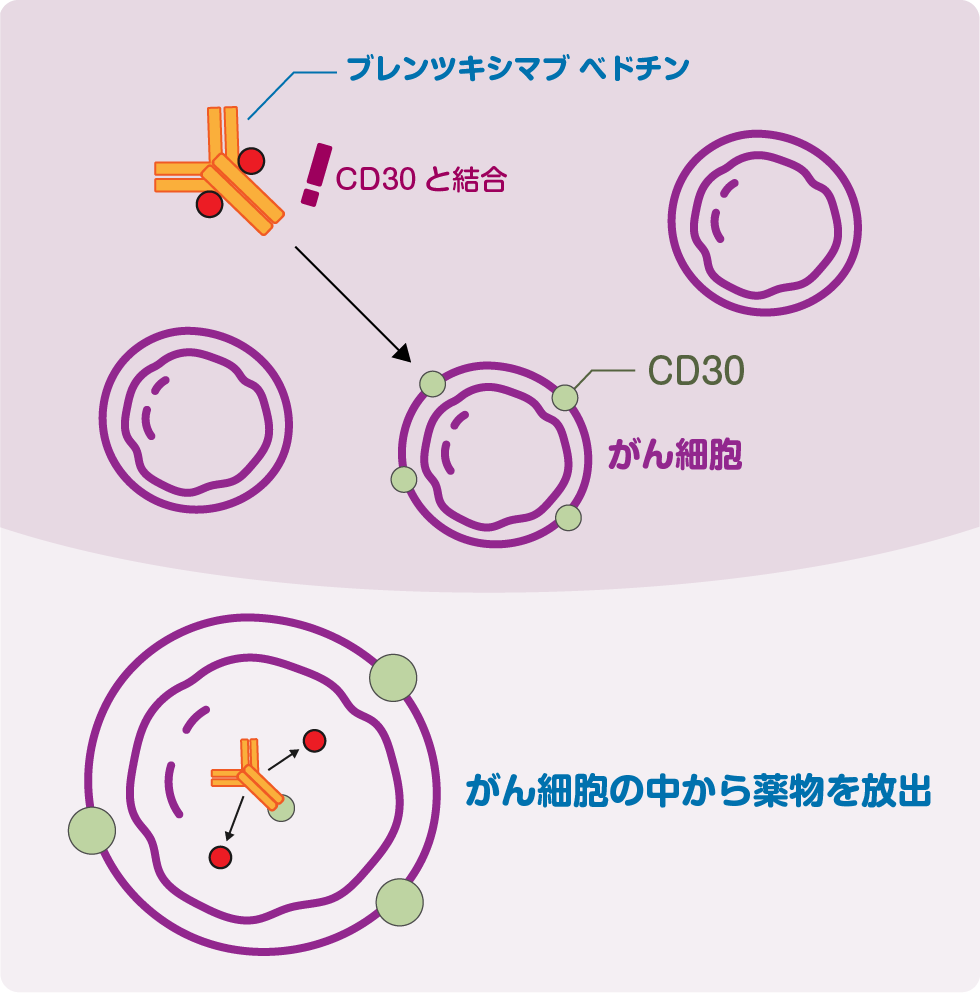
小児がんに治療薬が使えるように
新薬が承認されるまでには、第Ⅰ相、第Ⅱ相、第Ⅲ相の治験(薬事承認のための臨床試験)が行われます。そして、これらの試験の結果をもとに承認申請が出されます。
「ブレンツキシマブ ベドチン」という薬は、成人にはすでに使えるように承認されていますが、小児でも使えるようにするためには、小児に対する効果や安全性を示すデータが必要です。ただし、この薬が使われる病気はとてもまれで、日本の小児だけで十分なデータを集めるのが難しい状況でした。
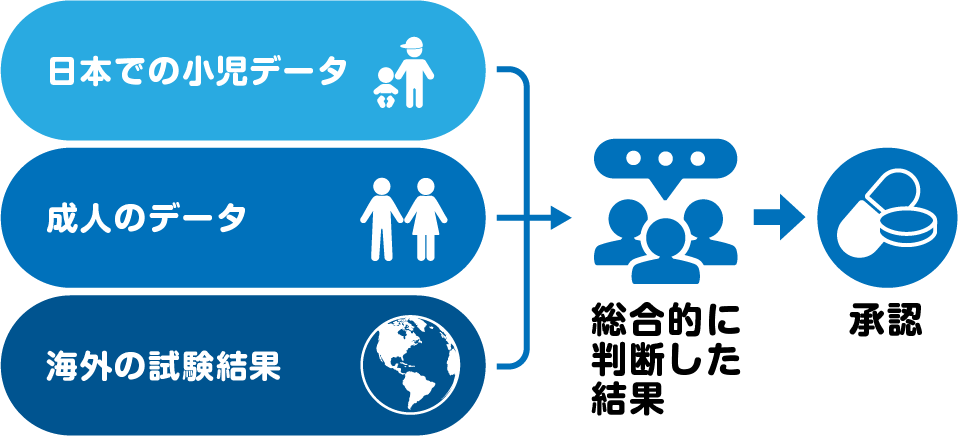
そこで小児での国内の薬の動きに関するデータ(薬物動態解析)を含む第Ⅰ相に加えて、海外の第Ⅰ/Ⅱ相、大人の第Ⅰ/Ⅱ相を含む他の試験結果を組み合わせて判断することで承認を得られました。
これらのデータをすべて組み合わせて判断することで、「ブレンツキシマブ ベドチン」は小児にも使える薬として承認されました。このように、データが集めにくい場合には、成人や海外のデータを活用することが大切です。
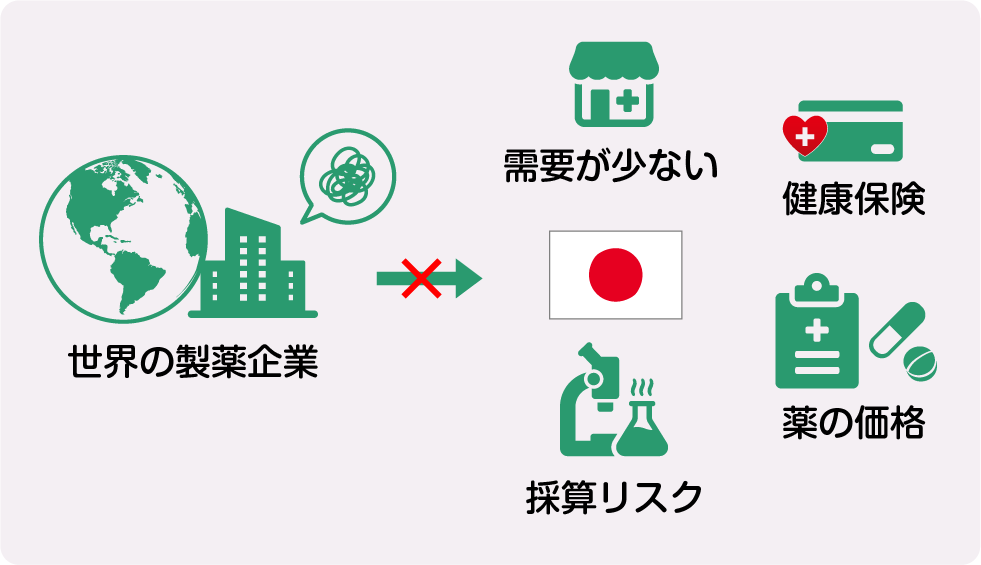
このようにして試験を行い、小児向けに薬を承認する方法は可能ですが、実際には試験に必要な資金を集めることが難しいのが現実です。そのため、試験を始めることや進めることがなかなかできないという問題があります。
ブレンツキシマブ ベドチン「商品名:アドセトリス」
1982 年にCD30 が発見されてから様々な腫瘍細胞に発現することが明らかにされました。これを標的にした治療薬として米国で「ブレンツキシマブ ベドチン」という薬が開発されました。この薬は、再発及び難治性CD30 陽性ホジキンリンパ腫及び全身性未分化大細胞リンパ腫を対象に2006 年から臨床試験が始まり、2011年米国にて治療薬として承認されました。日本では2011年から成人治験が行われ2014年に承認されました。その後、2016年には小児治験が始まり、2019年に小児にも使えるよう承認されました。


日本医師会の資金提供とメーカーからの試験用の薬の提供
日本には「日本医師会の治験推進センター」という仕組みがあります。これは、厚生労働省の研究費や、その後にできた「日本医療研究開発機構(AMED)」という機関の資金を使って運営されています。この治験推進センターに、名古屋医療センターの堀部敬三医師が応募し、採択されました。
さらに、製薬会社から薬の提供を受け、患者さんの同意を得た上で、医療施設の協力を得ながら治験が行われました。
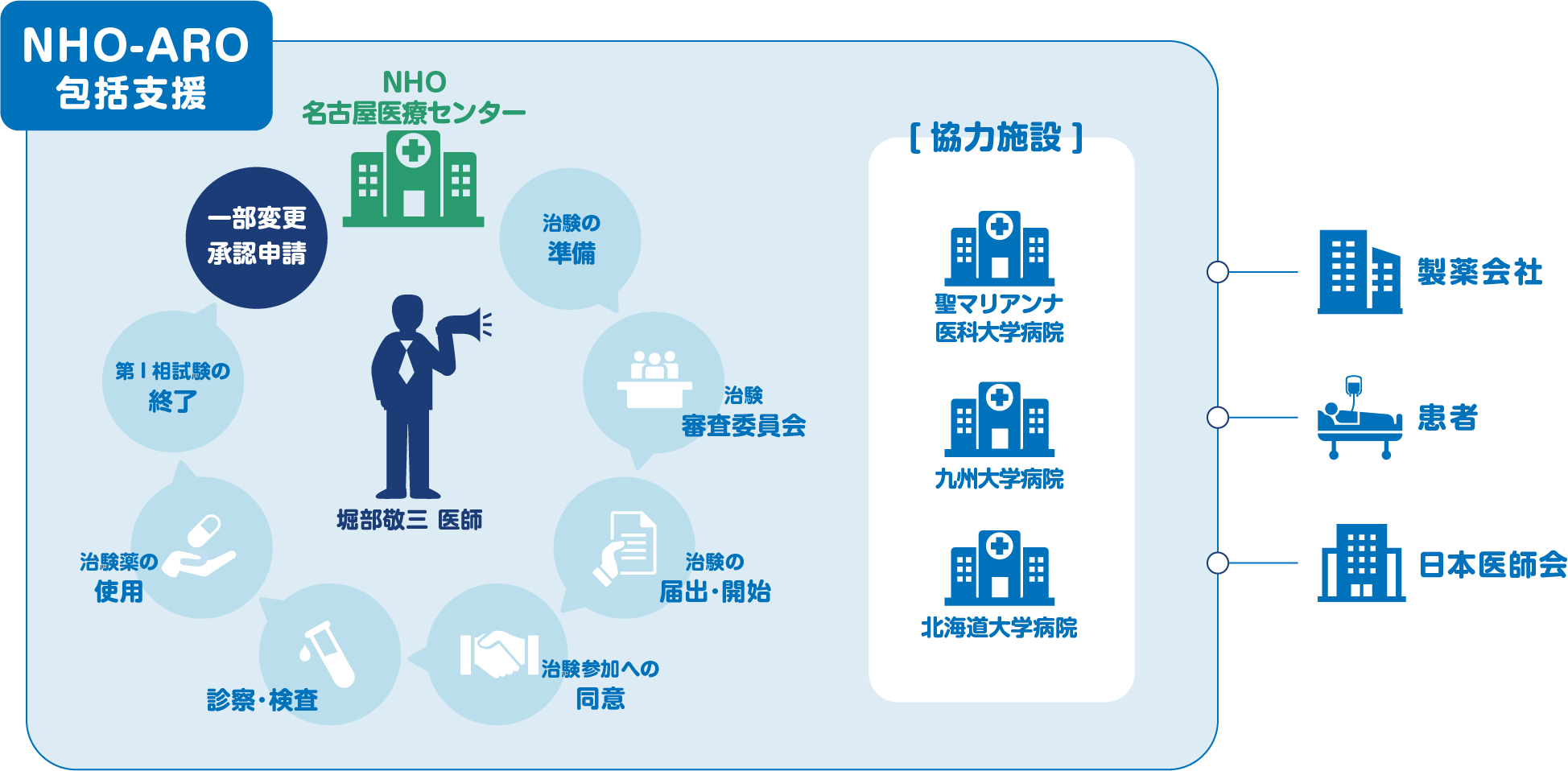
こうして第I相試験は2019年に終了し、結果をもとに2019年3月に武田薬品工業株式会社より、小児の再発または難治性のCD30陽性ホジキンリンパ腫および全身性未分化大細胞リンパ腫患者さんを対象とした「アドセトリス」に小児の用法及び用量を追加する変更承認申請し、2019年12月に小児の「再発または難治性のCD30陽性ホジキンリンパ腫および末梢性T細胞リンパ腫」(※1)に対する小児の用法用量に関する製造販売承認事項一部変更承認を取得しました。
※1 末梢性T細胞リンパ腫はECHELON-2 臨床第Ⅲ相試験でおこなわれた治験によるものです
製品名:アドセトリス/一般名: ブレンツキシマブ ベドチン